
2023年9月12日,Exelixis和英矽智能共同宣布,双方已签署一项独家许可协议,Exelixis将获得英矽智能ISM3091项目的全球开发和商业化权利。
ISM3091是一款潜在同类最佳(best-in-class)小分子抑制剂,靶向BRCA突变肿瘤的合成致死靶点USP1。
根据协议条款,英矽智能将授予Exelixis开发和商业化ISM3091及其他靶向USP1化合物的全球独家许可,并在2023年第三季度获得8000万美元的预付款。
此外,英矽智能还有资格获得后续基于临床开发、商业化和销售的里程碑付款,以及未来产品净销售额的分级版税。
这项许可协议是亚太地区的人工智能药物开发公司首次完成AI药物的对外授权交易,而8000万美金的首付款亦为今年生物医药领域小分子药物出海首付款最高的项目。
此前AI制药对外绝大多数为研发合作,本次英矽智能大额首付款的license out,也是新商业模式的里程碑事件。
 立项到license out,仅过去两年左右
立项到license out,仅过去两年左右
“合成致死”策略,是近年肿瘤新药开发的热门方向。USP1(泛素特异性蛋白酶1)则是该方向高度关注的抗肿瘤靶点,USP1在各种DNA损伤修复过程中发挥重要作用。
USP1抑制剂则拥有广泛治疗癌症的潜力。2023年7月,罗氏引进了KSQ Therapeutics的KSQ-4279,这是一款强效选择性小分子USP1抑制剂,目前正在进行治疗实体瘤的1期临床试验。
从时间上来看,英矽智能于2021年6月启动USP1项目,从立项到成功license out仅用了两年多时间。
2022年4月,英矽智能宣布提名靶向USP1的临床前候选化合物ISM3091用于抗肿瘤治疗。该候选化合物是一款由AI设计、并于9个月内成功提名临床前候选化合物,仅合成和测试不到80个化合物。
2023年4月,英矽智能宣布自主研发的USP1小分子抑制剂ISM3091已获得美国食品药品监督管理局(FDA)新药临床试验申请(Investigational New Drug Application,IND)批件,用于在实体瘤患者中开展I期临床试验。
2023年7月,国家药品监督管理局药品审评中心(CDE)官网显示,英矽智能 USP1小分子抑制剂ISM3091已获临床试验默示许可,用于晚期实体瘤治疗。
目前,全球针对USP1靶点的进展最快为I期临床,包括英矽智能的ISM3091和罗氏的KSQ-4279,其他绝大多数处于临床前。
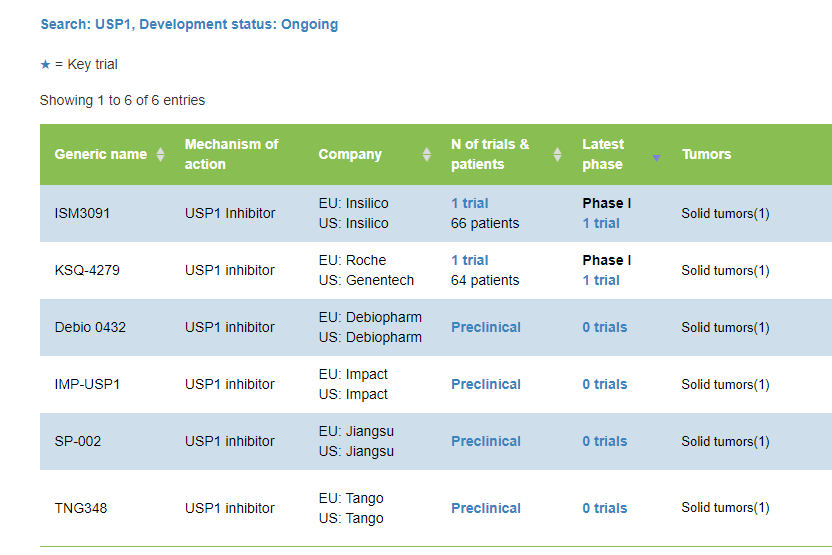
图:全球在研USP1抑制剂格局
 Exelixis为何选择英矽智能?
Exelixis为何选择英矽智能?
Exelixis成立于1994年,是一家专注肿瘤学、成功商业化的上市生物技术公司,致力于加速难以治疗癌症的新药的发现、开发和商业化。
公司已有多款上市药物,其中主打药物为卡博替尼(Cabozantinib),这是一款多靶点酪氨酸酶抑制剂,于2012 年11月在美国上市。
Exelixis正在积极通过license in的方式补充其研发管线,包括收购Cybrexa的一款多肽偶联药物,以及获得Sairopa B.V.针对SIRPα的潜在同类最佳单克隆抗体ADU-1805等。
关于此次交易,公司发现和转化研究执行副总裁兼首席科学官 Dana Aftab 博士表示:“我们相信 ISM3091 的有效抗肿瘤活性、耐受性和药代动力学的临床前数据使该化合物有别于竞争性 USP1 抑制剂,并使其成为 Exelixis 不断增长的临床阶段管道的重要补充。”
在FDA批准ISM3091的IND申请后,Exelixis计划在年底前加快在额外中心的临床1期试验的招募。
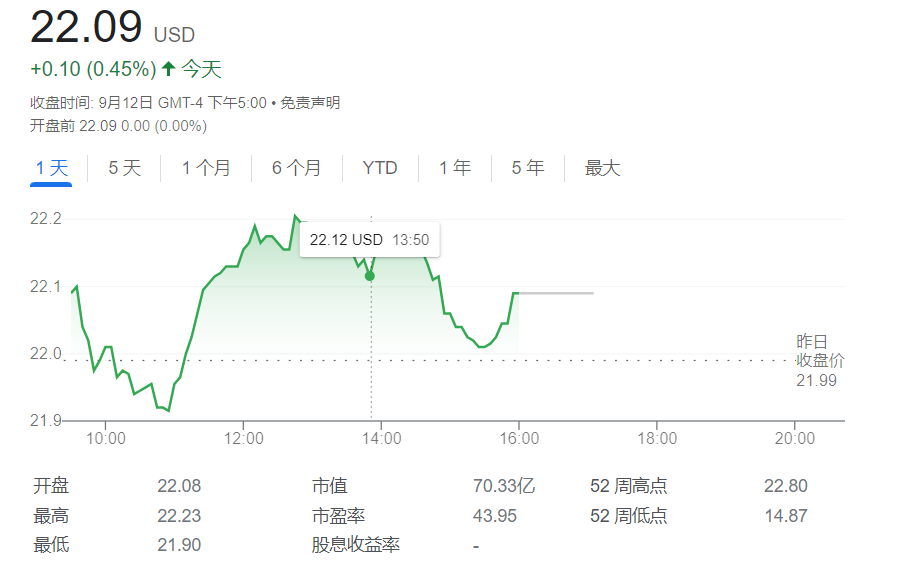
宣布引进消息后,Exelixis的股价并未有明显波动,该药物仍然处于I期临床阶段,期待未来有更多好消息发生。






 ufabet
มีเกมให้เลือกเล่นมากมาย: เกมเดิมพันหลากหลาย ครบทุกค่ายดัง
ufabet
มีเกมให้เลือกเล่นมากมาย: เกมเดิมพันหลากหลาย ครบทุกค่ายดัง


