今天为大家介绍的是来自Jan Kihlberg团队的一篇论文。分子变色龙具有一种灵活性,使它们能够根据环境的属性动态地遮蔽或暴露极性功能团。尽管分子变色龙的概念早在1970年就已引入,但自2010年代以来,随着药物发现越来越多地关注新的化学方式,对它们的兴趣显著增长。这些新的化学方式包括环状肽、大环和蛋白水解靶向嵌合体,它们都位于远离传统小分子药物的化学空间。药物的口服吸收需要细胞渗透性和水溶性。将这些属性以及强效的靶标结合引入到更大的新方式中,比对传统小分子药物来说是一个更加艰巨的任务。变色龙适应不同环境的能力可能对成功至关重要。

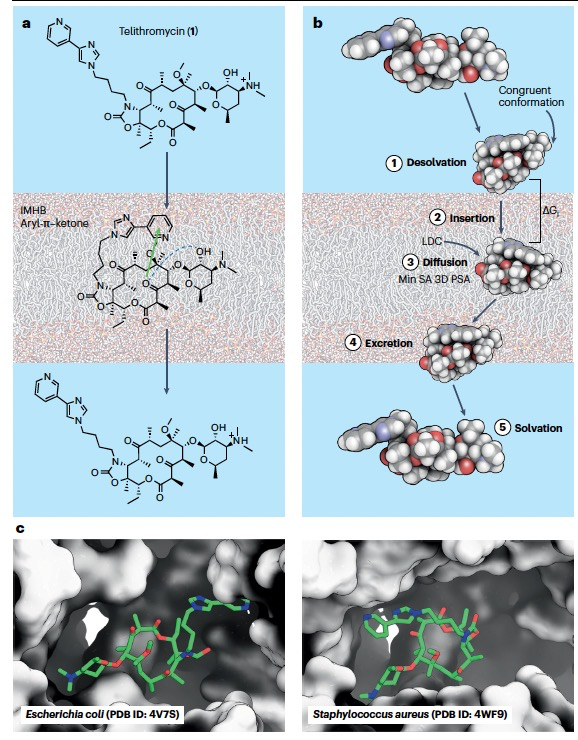
图 1
特定类别的有机分子,包括一些聚合物,能够在极性溶剂中暴露极性基团,在非极性溶剂中通过形成分子内相互作用来减少极性,从而发生构象变化,这种性质在1970年就已被描述为“变色龙特性”。在1991年,这个概念被引入到药物化学中,以解释这样一个令人惊讶的观察结果:两个看似极性的吗啡葡萄糖醛酸代谢物能够穿过血脑屏障并诱导镇痛。化合物能够改变它们的构象,以便在水溶液中暴露极性基团,但在非极性环境中通过形成非键合的分子内相互作用被掩埋,例如在脂质双层中,构成了当前接受的分子变色龙的定义。这种能力使分子变色龙既能显示高水溶性,也能显示高细胞渗透性,如抗菌剂泰利霉素所示(图1)。相比之下,不适应环境极性的刚性化合物更可能仅显示这些性质中的一种,如克虫单胞菌抑制剂所示。分子变色龙特性对于较大的药物比较小的药物更为重要。这可以从药物需要具有一定的水溶性以到达它们的靶标这一要求中理解,这意味着药物必须包含更多的极性基团来平衡非极性基团。当穿过脂质细胞膜时,去溶剂化极性基团所需的能量惩罚随着分子大小的增加而增加,限制了更高分子量时的细胞渗透性。分子变色龙可能通过在进入细胞时形成极性功能基团之间的互补性分子内相互作用,然后在细胞内再次暴露它们来打破这种“恶性关联”。估计约有50%的具有药物样性质的生物活性化合物可能表现为分子变色龙。分子变色龙的构象灵活性也可能对靶标结合很重要,允许一些变色龙结合到相关但结构不同的靶标。例如,芳香侧链的显著灵活性以及大环核心的一些灵活性允许泰利霉素结合到至少五种不同的细菌的核糖体,因此显示出广谱抗菌活性。
作用机理
为了口服给药,除了药效之外,药物必须具备三个关键属性:它必须能在肠液中溶解,它必须能穿透肠上皮细胞进入细胞内达到细胞内靶标,且其在肝脏中的代谢速度必须慢。对药物候选物的回顾性分析揭示,当它们位于由“Lipinski的五规则”所界定的化学空间内时,它们更有可能在口服后被吸收,该规则为大小、极性和亲脂性设定了上限指导值。或者,Veber规则定义的极性和柔韧性的截止值界定了口服生物可利用药物候选物的化学空间。这两组“规则”或描述符提供了首个指示,即一个化合物是否可通过口服给药。
估计只有20-50%与人类疾病相关的蛋白质可被位于Ro5和Veber规则内的小分子调节。然而,分析揭示,位于Ro5之外的化学空间的化合物为调节具有大的、平的和沟状结合位点的靶标提供了改善的机会,这些位点对于遵守Ro5的药物来说是无法触及的。位于Ro5之外的化学空间的药物也可以显示出令人满意的口服生物可利用性,据推测它们通常表现为分子变色龙。从历史上看,超出Ro5空间的口服药物主要来源于天然产物,但在过去10-20年中,‘从头开始’设计的药物越来越多。我们对使分子变色龙性成为可能的结构特征的理解还处于初级阶段,但在过去10-20年中对药物、类药物化合物和环状肽的研究开始识别一些关键原则。由于分子变色龙性源于化合物在生物学相关环境中所占据的不同构象的属性,所以变色龙性无法通过Ro5和Veber规则的描述符来描述。相反,描述变色龙性需要从它们构象的三维结构中计算出来的描述符。因此,回转半径(Rgyr)是比分子量更好的大小描述符,而三维极性表面积和可溶剂接触的三维极性表面积(SA 3D PSA)是比氢键供体和氢键受体计数或TPSA更好的极性测量。分子内氢键(IMHBs)的数量,尤其是在非极性环境中形成并在水环境中断裂的动态IMHBs,是另一个重要的极性描述符。分子亲脂性潜力和化合物的最大连续疏水表面片段是已被提出的亲脂性描述符,比logp计算的分配系数更相关。
在机制上,化合物从细胞外水环境穿过脂质细胞膜到细胞内环境的转运可以被视为通过几个连续步骤发生的,正如基于泰利霉素的核磁共振(NMR)研究所示(图1b)。当化合物穿过围绕细胞的水环境和膜的疏水内部之间的界面时,会发生脱溶作用。对于分子变色龙来说,这一步伴随着从一个更极性的、开放的(延展的)构象集合向一个闭合的(折叠的)构象集合的转换,在这些构象中极性基团被分子内相互作用隐藏。因此,化合物的最小SA 3D PSA以及通常也包括Rgyr被减小。分子动力学(MD)模拟建议,开放和闭合的构象可能都会插入到细胞膜的头基团和脂质尾部之间的极性-非极性界面,在那里它们随后转换,以便只有闭合的构象以它们最长轴平行于膜中的脂质尾部的方式穿过膜。随着化合物进入胞质,这一系列事件被逆转。基于超出Ro5空间的一小组化合物,已经发展了不同的模型来预测分子变色龙的渗透性(图1b)。第一个这样的模型基于渗透性与将化合物在非极性环境中(低介电构象)的最低能量状态从水转移到膜内部的自由能(ΔGi)的相关性。第二个模型侧重于识别一个“一致的”构象——即在水和类膜介质中都存在的构象——作为渗透物。在第三个模型中,化合物构象集合中的一个构象所暴露的最小SA 3D PSA与细胞渗透性呈现相关性。需要进一步的调查来理解这些模型中的哪一个是否比其他模型更好地描述分子变色龙。
实验手段
通过测量它们的物理化学性质、X射线晶体学和核磁共振(NMR)光谱学,分子变色龙主要通过这三种实验方式研究。这三种方法在通量和它们提供的信息质量上有所不同。
1-辛醇和水之间的分配系数的对数(LogPoct)是化合物亲脂性的最常见测量指标,但它本身并不提供任何关于变色龙性的信息。然而,对于匹配分子对的比较,即一个化合物和一个不能形成IMHB的对照物之间的比较,1-辛醇和水之间的分配系数的对数与甲苯和水之间的分配系数的对数之间的差值(ΔLogPoct-tol)是化合物形成动态、环境依赖的IMHB的倾向的衡量。EPSA,一种测定极性的色谱法,也被用于确定分子内氢键的形成。EPSA依赖于匹配分子对的保留时间的比较。对于这两种方法,对于具有多个氢键供体和受体的化合物,数据解释变得困难。尽管有它们的局限性,ΔLogPoct-tol和EPSA提供了高通量的数据,在药物发现项目的优化阶段是有用的。使用色谱HPLC可以测定描述符Chamelogk,据报道可以半定量地分类未带电的分子变色龙和非变色龙化合物。Chamelogk描述了一个化合物在乙腈和水的混合物中采用开放的、极性构象的程度,以及当纯乙腈被用作洗脱剂时采用封闭的、非极性构象的程度。这个描述符可以在中高通量下确定,并且不依赖于匹配分子对的分析。就像ΔLogPoct-tol和EPSA一样,它不提供关于产生变色龙性的分子内相互作用的任何结构信息。
X射线晶体学提供了关于非键合的分子内相互作用原子尺度分辨率的结构信息。对小分子和蛋白质-配体晶体结构的分析增强了我们对分子变色龙的理解。在晶体结构数据库中的详尽搜索被研究人员用来导出涉及五元至八元伪环的IMHB的倾向,并识别在药物发现中每个环大小的相关拓扑结构。这些研究突出了灵活连接的芳香侧链和动态形成的分子内氢键在提供变色龙性方面特别有效。然而,由于晶体中的局部环境影响所采用的构象,因此对生物系统的解释需要谨慎。此外,检查与其蛋白质靶标复合物中配体的精炼质量至关重要。
核磁共振(NMR)光谱是描述溶液中柔性分子构象和动力学的首选方法。它提供了平均的可观测量,这些管测量不仅包括了每个构象在原子分辨率下的几何信息,还包括它们的比例。然后,通过对群体平均NMR数据的解卷积,得到溶液中的分子集合体。在不同极性溶液中对同一分子的研究,提供了关于化合物如何调整其结构以适应其环境的信息,即它在多大程度上表现得像分子变色龙。
分子变色龙特性、渗透性和溶解性
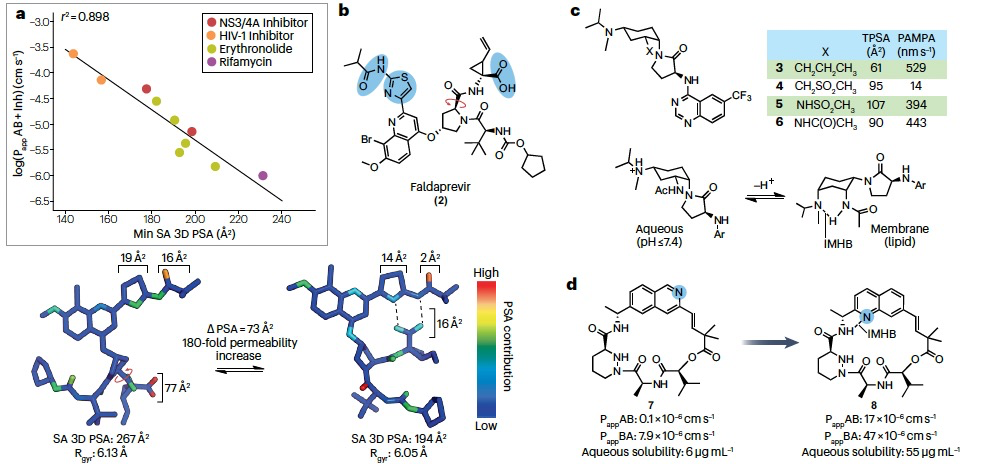
图 2
目前研究人员已经对一组具有高分子量的十种抗菌和抗病毒药物进行了研究,以探究不同构象的极性表面积如何与细胞渗透性和水溶性相关联,在这些药物中,分子变色龙特性可能很重要。X射线晶体学表明,这十种药物占据多种构象,使得可以确定不同描述符的极性表面积(PSA)与细胞渗透性或溶解性之间的关联(图2)。在结直肠腺癌细胞系Caco-2(Box 1)的单层细胞中,受抑制的(被动的)渗透性与每种药物的最小SA 3D PSA强烈相关(r² = 0.90),但与药物的TPSA相关性较低(r² = 0.36)。因此,药物采取最小化其PSA的构象的能力决定了这组药物的被动细胞渗透性。热力学水溶性与分子PSA最相关,分子PSA对构象变化的敏感性低于SA 3D PSA。这被解释为表明化合物在水溶液中占据几种不同的构象,与脂质膜环境相反。SA 3D PSA与被动细胞渗透性之间的定量关联允许对分子变色龙特性可能对细胞渗透性的影响程度进行预测。C型肝炎病毒蛋白酶抑制剂faldaprevir就是一个说明性的例子,因为它采取了两种晶体构象,这两种构象在SA 3D PSA上显示出很大的差异(图2b)。
超出Ro5空间
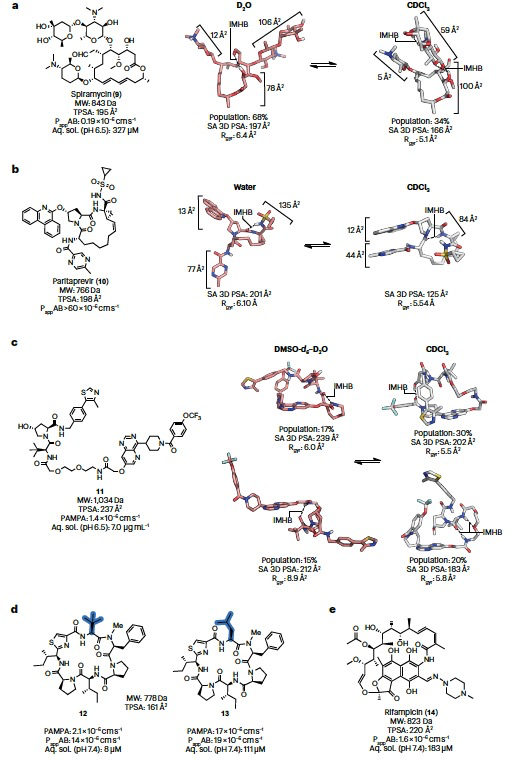
图 3
大环天然产物、从头设计的大环和非大环结构、蛋白质水解靶向嵌合体(PROTACs)和环状肽都位于超出Ro5空间,因此当作为口服药物使用时,它们很可能会从作为分子变色龙的特性中受益。大环天然产物通常调节难以用遵循Ro5规则的化合物进行药物化的靶标,而且已经发现它们中的一些是分子变色龙。环孢素A是一种免疫抑制剂,作为分子粘合剂,通常被认为是典型的分子变色龙。螺旋霉素的抗菌活性,以及罗红霉素和泰利霉素的抗菌活性,涉及抑制50S细菌核糖体亚基。螺旋霉素具有较高的热力学水溶性,但在Caco-2细胞中的渗透性较低,导致其生物利用度为35%(图3a)。核磁共振光谱显示,螺旋霉素的水相集合体主要由一个开放的主要构象占据,SA 3D PSA较高,在这个构象中,两个糖类彼此和大环核心相隔较远。在CDCl3中,螺旋霉素采用了两个类似的主要闭合构象。这些分子内相互作用导致两个CDCl3构象的SA 3D PSA比水中的构象降低了20-30 Ų。螺旋霉素在水中的主要构象与结合在大肠杆菌核糖体上的螺旋霉素相同,而与结合在Haloarcula marismortui核糖体的复合物中的一个次要构象相同。对于螺旋霉素,与水相比,氯仿中所采用的单一闭合构象也形成了额外的分子内氢键。在氯仿中,罗红霉素的两个糖类也相互堆叠,进一步减少了PSA,而在水溶液中,它们像螺旋霉素一样相互分离。对于泰利霉素,从水到非极性环境的过渡时,极性和尺寸(由Rgyr指示)通过芳香侧链折叠在大环上而降低。这种折叠似乎是由在侧链和去氧葡萄糖糖类之间形成的分子内氢键和范德华相互作用驱动的,这两者都导致了SA 3D PSA的显著降低。因此,如环孢素A和三种抗菌药螺旋霉素、罗红霉素和泰利霉素所示,大自然已将分子变色龙演化成为能够到达传统Ro5遵守药物无法调节的细胞内靶标的有效药物。有趣的是,对一个自然产物启发的大环库的研究揭示了变色龙特性已经被捕捉到库中的一些成员的设计中。
大环药物帕利他韦与NS3/4A蛋白酶的相对平坦的结合位点结合,并且是治疗C型肝炎病毒感染的联合治疗中的重要组成部分。就像非大环NS3/4A蛋白酶抑制剂法达普雷韦(图2b)一样,帕利他韦的TPSA超过140 Ų,表明分子变色龙特性是其高细胞渗透性的可能解释(图3b)。晶体结构检查和计算构象分析表明,帕利他韦在水中占据一个开放构象。尽管这种构象包含一个分子内氢键,但由于酰基磺酰胺基团和临近吡嗪环的酰胺键的氧原子暴露,其SA 3D PSA较高。在非极性环境中,帕利他韦通过两个芳香环的堆叠和其分子内氢键模式的调整,转换为能量上更有利的闭合构象。因此,酰基磺酰胺基团的三个氧原子被大环的烷基和环丙基群遮蔽,导致SA 3D PSA大幅降低。核磁共振光谱表明,另外两种C型肝炎病毒NS3/4A蛋白酶抑制剂西美普瑞和阿苏那普瑞以及HIV蛋白酶抑制剂阿塔那韦,在极性和非极性溶剂中都显示出很大的灵活性。这种灵活性转化为每个构象集合内SA 3D PSA的巨大差异,但并未转化为每种药物在极性和非极性溶剂中所采用的集合之间的显著差异。表现出这种行为的化合物被描述为“部分分子变色龙”,并提出它们采用低极性构象的能力有助于它们的细胞渗透性和口服吸收,类似于“完整”分子变色龙。
编译|曾全晨
审稿|王建民
参考资料
Poongavanam, V., Wieske, L.H.E., Peintner, S. et al. Molecular chameleons in drug discovery. Nat Rev Chem 8, 45–60 (2024).
https://doi.org/10.1038/s41570-023-00563-1



 ufabet
มีเกมให้เลือกเล่นมากมาย: เกมเดิมพันหลากหลาย ครบทุกค่ายดัง
ufabet
มีเกมให้เลือกเล่นมากมาย: เกมเดิมพันหลากหลาย ครบทุกค่ายดัง


